Thông tin sản phẩm
Hướng dẫn sử dụng
| Mọi thông tin dưới đây đã được Dược sĩ biên soạn lại. Tuy nhiên, nội dung hoàn toàn giữ nguyên dựa trên tờ Hướng dẫn sử dụng, chỉ thay đổi về mặt hình thức. |
1. Thành phần
Mỗi bơm tiêm đóng sẵn chứa 234 mg paliperidone palmitate trong 1,5 mL tương đương với 150 mg paliperidone.
Thành phần tá dược:
Polysorbate 20, polyethylene glycol 4000, acid citric monohydrate, dinatri hydrogen phosphate khan, natri dihydrogen phosphate monohydrate, natri hydroxide (để điều chỉnh pH), nước pha tiêm.
2. Công dụng (Chỉ định)
INVEGA SUSTENNA được chỉ định để điều trị duy trì bệnh tâm thần phân liệt ở bệnh nhân người lớn điều trị ổn định với paliperidone hoặc risperidone.
Ở một số bệnh nhân người lớn mắc tâm thần phân liệt và đáp ứng trước đó với paliperidone hoặc risperidone dùng đường uống, có thể sử dụng INVEGA SUSTENNA mà không cần điều trị ổn định trước bằng đường uống nếu các triệu chứng loạn thần nhẹ tới trung bình và cần phải điều trị thuốc tiêm tác dụng kéo dài.
3. Cách dùng - Liều dùng
- Cách dùng
INVEGA SUSTENNA chỉ được dùng để tiêm bắp. Không dùng thuốc theo bất kỳ đường dùng nào khác. Cần tiêm thuốc chậm, sâu vào cơ delta hoặc cơ mông. Mỗi lần tiêm phải do cán bộ y tế thực hiện. Tiêm nguyên liều cho một lần. Không nên chia liều làm nhiều lần tiêm.
Các liều khởi đầu ngày 1 và ngày 8 phải được tiêm vào cơ delta để nhanh chóng đạt được nồng độ điều trị (xem mục 5.2). Sau liều khởi đầu thứ hai, các liều duy trì hàng tháng có thể được tiêm vào cơ delta hoặc cơ mông. Trong trường hợp đau chỗ tiêm, nên cân nhắc chuyển vị trí tiêm từ cơ mông sang cơ delta (và ngược lại) nếu khó chịu nơi tiêm không được dung nạp tốt (xem mục 4.8). Khuyến cáo tiêm luân phiên giữa bên trái và bên phải.
Tiêm thuốc vào cơ delta
Kích thước kim tiêm khuyến cáo để tiêm các liều ban đầu và liều duy trì INVEGA SUSTENNA vào cơ delta được xác định theo cân nặng của bệnh nhân. Đối với bệnh nhân cân nặng ≥ 90 kg, nên sử dụng kim cỡ 22 dài 1½ inch (38,1 mm x 0,72 mm). Đối với bệnh nhân cân nặng < 90 kg, nên sử dụng kim cỡ 23 dài 1 inch (25,4 mm x 0,64 mm). Cần tiêm luân phiên giữa hai cơ delta.
Tiêm thuốc vào cơ mông
Kích thước kim tiêm được khuyến cáo để tiêm các liều duy trì INVEGA SUSTENNA vào cơ mông là cỡ 22 dài 1½ inch (38,1 mm x 0,72 mm). Nên tiêm vào vùng một phần tư phía trên-ngoài của vùng cơ mông. Cần tiêm luân phiên giữa hai cơ mông.
Thao tác sử dụng:
Bước 1: Lắc kỹ ống tiêm trong tối thiểu 10 giây để đảm bảo hỗn dịch đồng nhất.
Bước 2: Chọn kim tiêm phù hợp.
Liều khởi đầu đầu tiên của INVEGA SUSTENNA (150 mg) sẽ được tiêm vào Ngày 1 vào cơ DELTA sử dụng kim để tiêm vào cơ DELTA. Liều khởi đầu thứ hai của INVEGA SUSTENNA (100 mg) cũng được tiêm vào cơ DELTA một tuần sau đó (Ngày 8) bằng cách sử dụng kim để tiêm vào cơ DELTA.
Nếu bệnh nhân chuyển từ tiêm risperidone tác dụng kéo dài sang INVEGA SUSTENNA, liều tiêm INVEGA SUSTENNA đầu tiên (trong khoảng từ 25 mg đến 150 mg) có thể được tiêm vào cơ DELTA hoặc cơ MÔNG, sử dụng kim phù hợp cho vị trí tiêm vào thời điểm của liều tiêm kế tiếp theo dự kiến.
Sau đó, các liều tiêm duy trì hàng tháng có thể được tiêm vào cơ DELTA hoặc cơ MÔNG, sử dụng kim phù hợp cho vị trí tiêm. Để tiêm vào cơ DELTA, nếu bệnh nhân cân nặng < 90 kg, sử dụng kim cỡ 23 dài 1 inch, (25,4 mm x 0,64 mm) (đốc kim có màu xanh); nếu bệnh nhân cân nặng ≥ 90 kg, sử dụng kim cỡ 22 dài 1½ inch, (38,1 mm x 0,72 mm) (đốc kim có màu xám). Để tiêm cơ MÔNG, sử dụng kim cỡ 22 dài 1½ inch, (38,1 mm x 0,72 mm) (đốc kim có màu xám).
Bước 3: Giữ ống tiêm với nắp đậy hướng lên trên, tháo nắp bơm tiêm cao su bằng cách xoay nhẹ.
Bước 4: Gỡ miếng đậy vỉ chứa kim an toàn khoảng một nửa chiều dài vỉ. Giữ vỏ kim, sử dụng phần miếng đậy bằng nhựa bị gỡ ra. Giữ bơm tiêm hướng lên trên. Gắn kim an toàn vào bơm tiêm bằng cách xoay nhẹ để tránh kim tiêm gãy hay hư hỏng. Luôn kiểm tra các dấu hiệu hư hỏng hoặc rò rỉ trước khi dùng ra.
Bước 5: Kéo vỏ kim ra khỏi kim bằng cách kéo thẳng ra. Không xoắn vỏ kim vì kim có thể bị nới lỏng ra khỏi bơm tiêm.
Bước 6: Giữ bơm tiêm đã gắn kim ở vị trí thẳng đứng để đuổi khí. Đuổi bọt khí khỏi bơm tiêm bằng cách ấn pit-tông cẩn thận về phía trước.
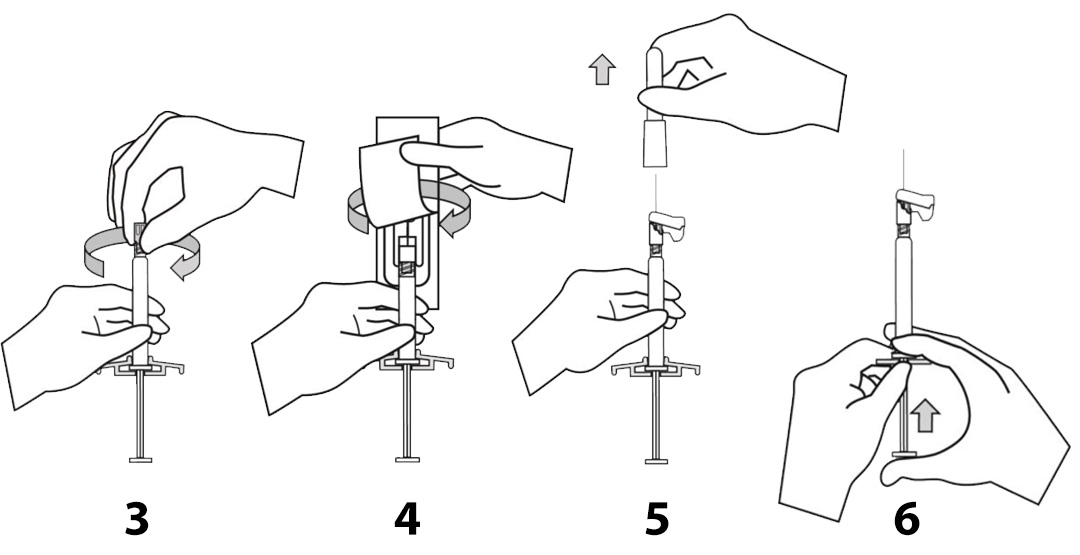
Bước 7: Tiêm toàn bộ lượng thuốc chậm, sâu vào cơ delta hoặc cơ mông đã được chọn của bệnh nhân. Không tiêm tĩnh mạch hoặc tiêm dưới da.
Bước 8: Sau khi tiêm xong, sử dụng ngón tay cái hoặc ngón tay trỏ của một tay (8a, 8b) hoặc mặt phẳng (8c) để kích hoạt hệ thống bảo vệ kim. Hệ thống được kích hoạt hoàn toàn khi nghe thấy một tiếng “click”. Vứt bơm tiêm có gắn kim đúng cách.
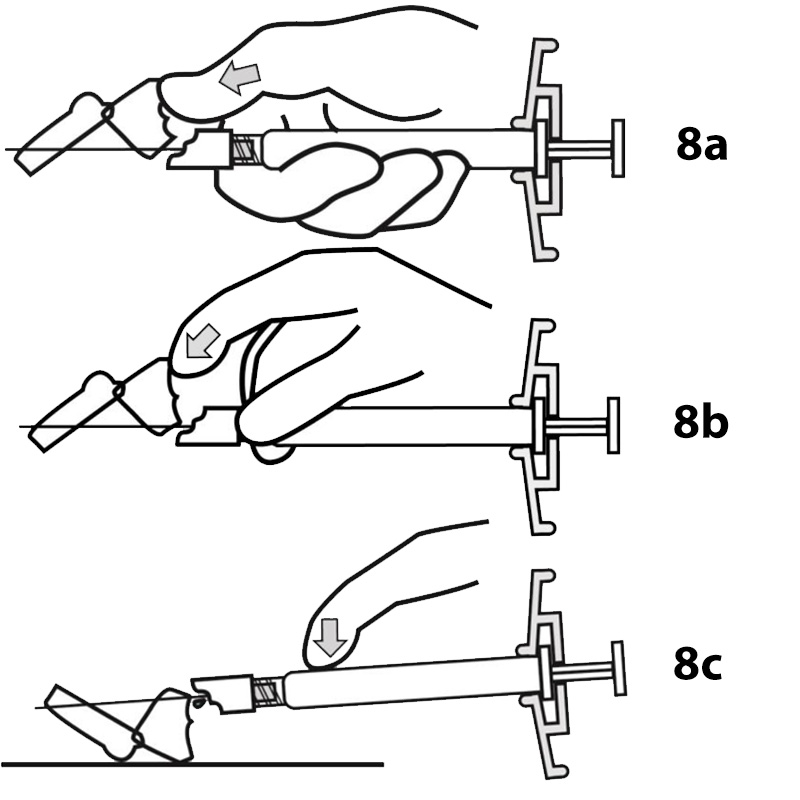
Bất kỳ phần thuốc không sử dụng hoặc chất thải nào cũng phải được xử lý phù hợp với yêu cầu của địa phương.
- Liều dùng
Liều khởi đầu khuyến cáo của INVEGA SUSTENNA là 150 mg vào ngày điều trị 1 và 100 mg một tuần sau đó (ngày 8), cả hai liều này đều tiêm vào cơ delta để nhanh đạt được nồng độ điều trị. Liều thứ ba nên được tiêm một tháng sau liều khởi đầu thứ hai. Liều duy trì hàng tháng khuyến cáo là 75 mg; một số bệnh nhân có thể có hiệu quả khi điều trị liều thấp hơn hoặc cao hơn trong phạm vi liều được khuyến cáo từ 25 đến 150 mg dựa trên khả năng dung nạp và/hoặc hiệu quả của mỗi bệnh nhân. Bệnh nhân thừa cân hoặc béo phì có thể cần liều ở khoảng cao hơn. Sau liều khởi đầu thứ hai, liều duy trì hàng tháng có thể tiêm hoặc vào cơ delta hoặc cơ mông.
Có thể điều chỉnh liều duy trì hàng tháng. Khi điều chỉnh liều, cần xem xét đặc tính giải phóng kéo dài của INVEGA SUSTENNA, vì hiệu quả đầy đủ của liều duy trì có thể không thể hiện rõ ràng trong vài tháng.
Chuyển từ paliperidone giải phóng kéo dài đường uống hoặc risperidone đường uống sang INVEGA SUSTENNA
Nên khởi đầu liều INVEGA SUSTENNA như mô tả ở đoạn đầu của mục 4.2 ở trên. Trong quá trình điều trị duy trì hàng tháng với INVEGA SUSTENNA, bệnh nhân trước đây đã ổn định với các liều khác nhau của paliperidone viên nén giải phóng kéo dài có thể đạt được nồng độ paliperidone ở trạng thái ổn định tương tự như đường tiêm. Để đạt được nồng độ ở trạng thái ổn định tương tự, các liều duy trì INVEGA SUSTENNA được chỉ ra như dưới đây:
Các liều paliperidone viên nén giải phóng kéo dài và liều cần thiết của INVEGA SUSTENNA để đạt được nồng độ paliperidone ở trạng thái ổn định tương tự trong điều trị duy trì | |
Liều trước đó của paliperidone viên nén giải phóng kéo dài | Thuốc tiêm INVEGA SUSTENNA |
3 mg hàng ngày | 25-50 mg hàng tháng |
6 mg hàng ngày | 75 mg hàng tháng |
9 mg hàng ngày | 100 mg hàng tháng |
12 mg hàng ngày | 150 mg hàng tháng |
Có thể ngừng uống paliperidone hoặc risperidone trước đó ở thời điểm bắt đầu điều trị INVEGA SUSTENNA. Một số bệnh nhân có thể có hiệu quả bằng giảm dần liều. Một số bệnh nhân chuyển từ liều cao hơn paliperidone đường uống (ví dụ, 9-12 mg hàng ngày) sang tiêm cơ mông INVEGA SUSTENNA có thể đạt được nồng độ trong huyết tương thấp hơn trong 6 tháng đầu sau khi chuyển. Vì thế, có thể cân nhắc tiêm vào cơ delta trong 6 tháng đầu.
Chuyển từ risperidone thuốc tiêm tác dụng kéo dài sang INVEGA SUSTENNA
Khi chuyển bệnh nhân từ sử dụng risperidone thuốc tiêm tác dụng kéo dài, bắt đầu điều trị INVEGA SUSTENNA thay cho liều tiêm kế tiếp dự kiến. Nên tiếp tục dùng INVEGA SUSTENNA cách nhau mỗi tháng. Không bắt buộc sử dụng phác đồ liều khởi đầu một tuần tiêm bắp (tương ứng tiêm vào ngày 1 và 8), như được mô tả ở trên. Bệnh nhân trước đây ổn định ở những liều khác nhau của risperidone thuốc tiêm tác dụng kéo dài có thể đạt được nồng độ paliperidone ở trạng thái ổn định tương tự trong quá trình điều trị duy trì với INVEGA SUSTENNA chế độ liều hàng tháng như sau:
Các liều risperidone thuốc tiêm tác dụng kéo dài và liều cần thiết của INVEGA SUSTENNA để đạt được nồng độ paliperidone ở trạng thái ổn định tương tự | |
Liều trước đó của risperidone thuốc tiêm tác dụng kéo dài | Thuốc tiêm INVEGA SUSTENNA |
25 mg mỗi 2 tuần | 50 mg hàng tháng |
37,5 mg mỗi 2 tuần | 75 mg hàng tháng |
50 mg mỗi 2 tuần | 100 mg hàng tháng |
Ngừng sử dụng các thuốc chống loạn thần phải được thực hiện phù hợp với thông tin kê đơn của mỗi thuốc. Nếu ngừng sử dụng INVEGA SUSTENNA, phải xem xét đặc tính giải phóng kéo dài của thuốc. Cần định kỳ đánh giá nhu cầu tiếp tục các thuốc điều trị triệu chứng ngoại tháp (EPS) đang dùng.
Đối tượng đặc biệt
Người cao tuổi
Hiệu quả và tính an toàn ở người cao tuổi > 65 tuổi chưa được xác lập. Nói chung, liều khuyến cáo của INVEGA SUSTENNA cho bệnh nhân cao tuổi có chức năng thận bình thường giống như bệnh nhân người lớn trẻ hơn có chức năng thận bình thường. Tuy nhiên, vì bệnh nhân cao tuổi có thể suy giảm chức năng thận, có thể cần điều chỉnh liều.
Suy thận
INVEGA SUSTENNA chưa được nghiên cứu một cách hệ thống trên bệnh nhân suy thận. Đối với bệnh nhân suy thận nhẹ (độ thanh thải creatinine ≥ 50 đến < 80 mL/phút), khuyến cáo bắt đầu điều trị INVEGA SUSTENNA liều 100 mg vào ngày điều trị 1 và 75 mg một tuần sau đó, cả hai liều đều tiêm vào cơ delta. Liều duy trì hàng tháng là 50 mg với khoảng liều từ 25 đến 100 mg dựa trên dung nạp và/hoặc hiệu quả của mỗi bệnh nhân. Không khuyến cáo dùng INVEGA SUSTENNA cho bệnh nhân suy thận trung bình hoặc nặng
(độ thanh thải creatinine < 50 mL/phút).
Suy gan
Dựa trên kinh nghiệm với paliperidone đường uống, không cần điều chỉnh liều ở bệnh nhân suy gan nhẹ hoặc trung bình. Paliperidone chưa được nghiên cứu ở bệnh nhân suy gan nặng, do đó cần thận trọng khi dùng thuốc cho những bệnh nhân này.
Bệnh nhân nhi
Tính an toàn và hiệu quả của INVEGA SUSTENNA trên trẻ em và thanh thiếu niên < 18 tuổi chưa được xác lập. Chưa có dữ liệu ở nhóm đối tượng này.
- Quên liều
Tránh quên liều
Khuyến cáo liều khởi đầu thứ hai của INVEGA SUSTENNA tiêm một tuần sau liều thứ nhất.
Để tránh quên liều, bệnh nhân có thể được tiêm liều thứ hai 4 ngày trước hoặc sau thời điểm một tuần (ngày8). Tương tự như vậy, liều tiêm thứ ba và các liều tiếp theo sau phác đồ liều khởi đầu được khuyến cáo tiêm hàng tháng. Để tránh quên liều hàng tháng, bệnh nhân có thể được tiêm vào thời điểm tối đa 7 ngày trước hoặc sau thời điểm hàng tháng.
Nếu quên ngày đã xác định cho liều tiêm INVEGA SUSTENNA thứ hai (ngày 8 ± 4 ngày), khuyến cáo tái khởi trị tùy thuộc khoảng thời gian đã quên tính từ liều tiêm đầu tiên của bệnh nhân.
Quên liều khởi đầu thứ hai (< 4 tuần kể từ liều tiêm đầu tiên)
Nếu dưới 4 tuần kể từ liều tiêm đầu tiên, bệnh nhân nên được tiêm liều thứ hai 100 mg vào cơ delta càng sớm càng tốt. Nên tiêm liều thứ ba INVEGA SUSTENNA 75 mg vào cơ delta hoặc cơ mông 5 tuần sau liều tiêm đầu tiên (bất kể thời gian tiêm liều thứ hai). Sau đó, nên tiếp tục chu kỳ tiêm hàng tháng bình thường liều 25 mg đến 150 mg vào cơ delta hoặc cơ mông dựa trên khả năng dung nạp và/hoặc hiệu quả của mỗi bệnh nhân.
Quên liều khởi đầu thứ hai (4-7 tuần kể từ liều tiêm đầu tiên)
Nếu từ 4 đến 7 tuần kể từ liều tiêm INVEGA SUSTENNA đầu tiên, bắt đầu dùng lại với 2 liều tiêm, mỗi liều 100 mg theo cách sau:
1. Tiêm một liều vào cơ delta càng sớm càng tốt
2. Tiêm một liều khác vào cơ delta một tuần sau đó
3. Bắt đầu lại chu kỳ tiêm hàng tháng bình thường liều 25 mg đến 150 mg vào cơ delta hoặc cơ mông dựa trên khả năng dung nạp và/hoặc hiệu quả của mỗi bệnh nhân.
Quên liều khởi đầu thứ hai (> 7 tuần kể từ liều tiêm đầu tiên)
Nếu quá 7 tuần kể từ liều tiêm INVEGA SUSTENNA đầu tiên, bắt đầu dùng liều như mô tả cho liều khởi đầu khuyến cáo của INVEGA SUSTENNA ở trên.
Quên liều duy trì hàng tháng (từ 1 tháng đến 6 tuần)
Sau khi bắt đầu điều trị, khuyến cáo chu kỳ tiêm INVEGA SUSTENNA hàng tháng. Nếu dưới 6 tuần kể từ liều tiêm cuối, nên dùng liều ổn định trước đó càng sớm càng tốt, sau đó tiêm liều hàng tháng.
Quên liều duy trì hàng tháng (> 6 tuần đến 6 tháng)
Nếu quá 6 tuần kể từ liều tiêm INVEGA SUSTENNA cuối cùng, khuyến cáo như sau:
Đối với bệnh nhân đã ổn định với liều từ 25 đến 100 mg
1. Tiêm vào cơ delta càng sớm càng tốt với cùng một liều mà bệnh nhân đã điều trị ổn định trước đó.
2. Tiêm thêm một liều khác vào cơ delta (cùng liều) một tuần sau đó (ngày 8).
3. Bắt đầu lại chu kỳ tiêm hàng tháng bình thường liều 25 mg đến 150 mg vào cơ delta hoặc cơ mông dựa trên khả năng dung nạp và/hoặc hiệu quả của mỗi bệnh nhân.
Đối với bệnh nhân đã ổn định với liều 150 mg
1. Tiêm một liều 100 mg vào cơ delta càng sớm càng tốt.
2. Tiêm thêm một liều 100 mg khác vào cơ delta một tuần sau đó (ngày 8).
3. Bắt đầu lại chu kỳ tiêm hàng tháng bình thường liều 25 mg đến 150 mg vào cơ delta hoặc cơ mông dựa trên khả năng dung nạp và/hoặc hiệu quả của mỗi bệnh nhân.
Quên liều duy trì hàng tháng (> 6 tháng)
Nếu quá 6 tháng kể từ liều tiêm INVEGA SUSTENNA cuối cùng, bắt đầu dùng liều như mô tả cho liều khởi đầu khuyến cáo của INVEGA SUSTENNA ở trên.
- Quá liều
Triệu chứng
Nói chung, các dấu hiệu và triệu chứng quá liều được ghi nhận là biểu hiện quá mức của các tác dụng dược lý đã biết của paliperidone, như buồn ngủ và an thần, nhịp tim nhanh và hạ huyết áp, kéo dài khoảng QT và các triệu chứng ngoại tháp. Đã có báo cáo xoắn đỉnh và rung thất ở một bệnh nhân dùng quá liều paliperidone đường uống. Trong trường hợp quá liều cấp, cần cân nhắc đến khả năng có liên quan của nhiều thuốc.
Điều trị
Cân nhắc đặc tính giải phóng kéo dài của thuốc và thời gian bán thải dài của paliperidone khi đánh giá nhu cầu điều trị và hồi phục. Không có chất giải độc đặc hiệu cho paliperidone. Cần thực hiện các biện pháp điều trị hỗ trợ thông thường. Thiết lập và duy trì đường thở thông thoáng, đảm bảo cung cấp đủ oxy và thông khí tốt.
Bắt đầu theo dõi tim mạch ngay lập tức và nên bao gồm theo dõi điện tâm đồ liên tục vì rối loạn nhịp tim có thể xảy ra. Điều trị hạ huyết áp và suy tuần hoàn bằng các biện pháp phù hợp như truyền dịch và/hoặc các thuốc cường giao cảm. Trong trường hợp xuất hiện triệu chứng ngoại tháp nặng, cần sử dụng các thuốc kháng cholinergic. Theo dõi và giám sát chặt chẽ cho đến khi bệnh nhân hồi phục.
4. Chống chỉ định
Quá mẫn với thành phần hoạt chất, với risperidone hoặc bất cứ tá dược nào được liệt kê.
5. Tác dụng phụ
Tóm tắt thông tin an toàn của thuốc
Các phản ứng có hại phổ biến nhất được báo cáo trong các thử nghiệm lâm sàng là mất ngủ, đau đầu, lo âu, nhiễm trùng đường hô hấp trên, phản ứng tại chỗ tiêm, hội chứng parkinson, tăng cân, chứng nằm ngồi không yên, kích động, an thần/ngủ gà, buồn nôn, táo bón, chóng mặt, đau cơ xương, nhịp tim nhanh, run, đau bụng, nôn, tiêu chảy, mệt mỏi và loạn trương lực cơ. Trong đó, chứng nằm ngồi không yên và an thần/ngủ gà dường như liên quan đến liều dùng.
Bảng liệt kê các phản ứng có hại
Dưới đây là tất cả các phản ứng có hại của paliperidone được báo cáo theo phân loại tần suất ước tính từ các thử nghiệm lâm sàng của paliperidone palmitate. Các thuật ngữ và tần suất được sử dụng như sau: rất thường gặp (≥ 1/10), thường gặp (≥ 1/100 đến < 1/10), ít gặp (≥ 1/1 000 đến < 1/100), hiếm gặp (≥ 1/10 000 đến < 1/1 000), rất hiếm gặp (< 1/10 000), và chưa rõ (không thể ước tính được từ các dữ liệu hiện có).
| Phân loại hệ cơ quan | Phản ứng có hại | ||||
| Tần suất | |||||
| Rất thường gặp | Thường gặp | Ít gặp | Hiếm gặp | Chưa rõa | |
| Nhiễm trùng và nhiễm ký sinh trùng | nhiễm trùng đường hô hấp trên, nhiễm trùng đường niệu, cúm | viêm phổi, viêm phế quản, nhiễm trùng đường hô hấp, viêm xoang, viêm bàng quang, nhiễm trùng tai, viêm amidan, nấm móng, viêm mô tế bào, áp xe dưới da | nhiễm trùng mắt, viêm da do bọ ve | ||
| Rối loạn máu và hệ bạch huyết | giảm số lượng bạch cầu, thiếu máu | giảm bạch cầu trung tính, giảm tiểu cầu, tăng số lượng bạch cầu ái toan | mất bạch cầu hạt | ||
| Rối loạn hệ miễn dịch | quá mẫn | phản ứng phản vệ | |||
| Rối loạn nội tiết | tăng prolactin máub | tiết hormone chống bài niệu không phù hợp, glucose niệu | |||
| Rối loạn chuyển hóa và dinh dưỡng | tăng đường huyết, tăng cân, giảm cân, giảm cảm giác ngon miệng | đái tháo đườngd, tăng insulin trong máu, tăng thèm ăn, chán ăn, tăng triglyceride máu, tăng cholesterol máu | nhiễm toan ceton trong đái tháo đường, hạ đường huyết, khát nhiều | ngộ độc nước | |
| Rối loạn tâm thần | mất ngủe | kích động, trầm cảm, lo âu | rối loạn giấc ngủ, hưng cảm, giảm ham muốn tình dục, căng thẳng, ác mộng | căng trương lực, tình trạng lú lẫn, mộng du, cảm xúc cùn mòn, mất khoái cảm | Rối loạn giấc ngủ liên quan đến ăn uống |
| Rối loạn hệ thần kinh | hội chứng parkinsonc, chứng nằm ngồi không yênc, an thần/ngủ gà, rối loạn trương lực cơc, chóng mặt, rối loạn vận độngc, run, đau đầu | rối loạn vận động muộn, ngất, tăng hoạt động tâm thần vận động, chóng mặt tư thế, rối loạn chú ý, rối loạn vận ngôn, rối loạn vị giác, giảm xúc giác, dị cảm | hội chứng ác tính do thuốc an thần kinh, thiếu máu não, không đáp ứng với kích thích, mất ý thức, giảm mức độ ý thức, co giậte, rối loạn thăng bằng, bất thường trong phối hợp vận động, chứng run lắc đầu cổ | hôn mê do đái tháo đường | |
| Rối loạn mắt | nhìn mờ, viêm kết mạc, khô mắt | tăng nhãn áp, rối loạn chuyển động mắt, đảo mắt, sợ ánh sáng, tăng tiết nước mắt, sung huyết nhãn cầu | hội chứng nhão mống mắt (phẫu thuật nội nhãn) | ||
| Rối loạn tai và mê đạo | chóng mặt, ù tai, đau tai | ||||
| Rối loạn tim | nhịp tim nhanh | block nhĩ thất, rối loạn dẫn truyền, kéo dài khoảng QT trên điện tâm đồ, hội chứng nhịp nhanh tư thế, chậm nhịp tim, điện tâm đồ bất thường, đánh trống ngực | rung nhĩ, rối loạn nhịp xoang | ||
| Rối loạn mạch | tăng huyết áp | hạ huyết áp, hạ huyết áp tư thế | tắc mạch phổi huyết khối tĩnh mạch, đỏ mặt | thiếu máu cục bộ | |
| Rối loạn hô hấp, lồng ngực và trung thất | ho, sung huyết mũi | khó thở, đau họng-thanh quản, chảy máu cam | hội chứng ngừng thở khi ngủ, sung huyết phổi, sung huyết đường hô hấp, có ran, khò khè | chứng thở quá nhanh, viêm phổi do hít phải, khàn tiếng | |
| Rối loạn tiêu hóa | đau bụng, nôn, buồn nôn, táo bón, tiêu chảy, chứng khó tiêu, đau răng | khó chịu ở bụng, viêm dạ dày ruột, khó nuốt, khô miệng, đầy hơi | viêm tụy, tắc ruột, sưng lưỡi, đại tiện không tự chủ, u phân, viêm môi | liệt ruột | |
| Rối loạn gan mật | tăng transaminase | tăng gamma-glutamyltransferase, tăng men gan | vàng da | ||
| Rối loạn da và mô dưới da | mày đay, ngứa, phát ban, rụng tóc, chàm, da khô, ban đỏ, mụn trứng cá | phát ban do thuốc, dày sừng, viêm da tiết bã, gàu | Hội chứng Stevens-Johnson/hoại tử thượng bì nhiễm độc, phù mạch, mất màu da | ||
| Rối loạn cơ xương và mô liên kết | đau cơ xương, đau lưng, đau khớp | tăng creatine phosphokinase máu, co cơ, cứng khớp, yếu cơ | tiêu cơ vân, sưng khớp | bất thường tư thế | |
| Rối loạn thận và tiết niệu | tiểu không tự chủ, tiểu rắt, tiểu khó | bí tiểu | |||
| Giai đoạn mang thai, hậu sản và chu sinh | hội chứng cai thuốc trên trẻ sơ sinh | ||||
| Rối loạn vú và hệ sinh sản | vô kinh | rối loạn cương dương, rối loạn xuất tinh, rối loạn kinh nguyệte, vú to ở nam giới, tăng tiết sữa, rối loạn tình dục, đau vú | cương dương, khó chịu ở vú, căng đau ở vú, vú to, khí hư âm đạo | ||
| Rối loạn toàn thân và tại chỗ tiêm | sốt, suy nhược, mệt mỏi, phản ứng tại chỗ tiêm | phù mặt, phùe, tăng thân nhiệt, dáng đi bất thường, đau ngực, tức vùng ngực, cảm giác khó chịu, chai cứng chỗ tiêm | hạ thân nhiệt, ớn lạnh, khát, hội chứng cai thuốc, áp xe tại vị trí tiêm, viêm mô tế bào tại vị trí tiêm, nang tại vị trí tiêm, máu tụ tại vị trí tiêm | giảm thân nhiệt, hoại tử tại vị trí tiêm, loét tại vị trí tiêm | |
| Chấn thương, ngộ độc và biến chứng thủ thuật | té ngã | ||||
a Tần suất của các phản ứng có hại này được xác định là "chưa rõ" vì không quan sát thấy trong các thử nghiệm lâm sàng của paliperidone palmitate. Các phản ứng này thu được từ báo cáo tự phát sau khi lưu hành thuốc và tần suất không thể xác định được, hoặc thu được từ dữ liệu thử nghiệm lâm sàng của risperidone (bất kỳ dạng bào chế nào) hoặc của paliperidone đường uống và/hoặc các báo cáo sau khi lưu hành thuốc. b Tham khảo mục 'Tăng prolactin máu' dưới đây. c Tham khảo mục 'Triệu chứng ngoại tháp' dưới đây. d Trong các thử nghiệm đối chứng với giả dược, đái tháo đường được báo cáo ở nhóm dùng INVEGA SUSTENNA là 0,32% so với tỷ lệ 0,39% ở nhóm dùng giả dược. Tỷ lệ mắc nói chung của tất cả các thử nghiệm lâm sàng là 0,65% ở tất cả các đối tượng được điều trị với INVEGA SUSTENNA. e Mất ngủ bao gồm: mất ngủ đầu giấc, mất ngủ giữa giấc; Co giật bao gồm: co giật cơn lớn; Phù bao gồm: phù toàn thân, phù ngoại biên, phù ấn lõm. Rối loạn kinh nguyệt bao gồm: chậm kinh nguyệt, kinh nguyệt không đều, thiểu kinh. | |||||
Các tác dụng không mong muốn ghi nhận với chế phẩm risperidone
Paliperidone là chất chuyển hóa có hoạt tính của risperidone, do đó, các dữ liệu về phản ứng có hại của các chất này (bao gồm cả dạng đường uống và tiêm) có thể áp dụng cho nhau.
Mô tả một số phản ứng có hại chọn lọc
Phản ứng phản vệ
Hiếm có báo cáo trường hợp phản ứng phản vệ sau khi tiêm INVEGA SUSTENNA trong quá trình lưu hành thuốc trên bệnh nhân đã từng dung nạp risperidone đường uống hoặc paliperidone đường uống.
Phản ứng tại chỗ tiêm
Phản ứng có hại thường gặp nhất được báo cáo liên quan đến vị trí tiêm là đau. Phần lớn các phản ứng này được báo cáo ở mức độ nhẹ đến trung bình. Đánh giá chủ quan đau tại vị trí tiêm dựa trên thang VAS (visual analogue scale) có khuynh hướng giảm tần suất và cường độ theo thời gian trong tất cả các nghiên cứu pha 2 và 3 với INVEGA SUSTENNA. Tiêm vào cơ delta được nhận thấy hơi đau hơn so với tiêm vào cơ mông. Các phản ứng khác tại chỗ tiêm hầu hết đều có mức độ nhẹ và bao gồm chai cứng (thường gặp), ngứa (ít gặp) và nốt sẩn (hiếm gặp).
Triệu chứng ngoại tháp (EPS)
EPS được đưa vào một phân tích tổng hợp các thuật ngữ sau: hội chứng parkinson (bao gồm tăng tiết nước bọt, cứng cơ xương, hội chứng parkinson, chảy nước dãi, cứng cơ kiểu bánh răng, vận động chậm chạp, giảm khả năng vận động, hiện tượng mặt nạ, căng cơ, mất vận động, cứng gáy, cứng cơ, dáng đi kiểu parkinson, bất thường phản xạ mũi mi và run khi nghỉ ngơi kiểu parkinson), chứng nằm ngồi không yên (bao gồm nằm ngồi không yên, không nghỉ, tăng vận động và hội chứng chân không nghỉ), rối loạn vận động (rối loạn vận động, giật cơ, chứng múa giật múa vờn, chứng múa vờn và giật rung cơ), rối loạn trương lực cơ (bao gồm rối loạn trương lực cơ, tăng trương lực, vẹo cổ, co cơ không tự chủ, co cứng cơ, co thắt mi mắt, xoay mắt, lưỡi tê liệt, co thắt cơ mặt, co thắt thanh quản, tăng trương lực cơ, cong ưỡn người ra sau, co thắt hầu họng, cong người sang bên, co thắt vùng lưỡi và cứng hàm), và run.
Lưu ý danh sách trên bao gồm một hoạt phổ rộng hơn các triệu chứng, không nhất thiết phải có nguồn gốc ngoại tháp.
Tăng cân
Trong nghiên cứu 13 tuần liên quan đến liều khởi đầu 150 mg, tỷ lệ bệnh nhân tăng cân bất thường ≥ 7% cho thấy xu hướng liên quan đến liều, với tỷ lệ mắc 5% ở nhóm dùng giả dược so với tỷ lệ 6%, 8% và 13% lần lượt trong nhóm INVEGA SUSTENNA 25 mg, 100 mg và 150 mg.
Trong giai đoạn 33 tuần chuyển tiếp/duy trì nhãn mở của thử nghiệm dự phòng tái phát dài hạn, 12% bệnh nhân điều trị INVEGA SUSTENNA đạt tiêu chuẩn này (tăng cân ≥ 7% từ giai đoạn mù đôi đến kết thúc); sự thay đổi cân nặng trung bình (SD) so với trước giai đoạn nhãn mở ban đầu là + 0,7 (4,79) kg.
Tăng prolactin máu
Trong các thử nghiệm lâm sàng, đã ghi nhận tăng trung vị nồng độ prolatin huyết thanh ở bệnh nhân cả hai giới dùng INVEGA SUSTENNA. Các phản ứng có hại gợi ý tăng nồng độ prolactin (như vô kinh, tăng tiết sữa, rối loạn kinh nguyệt, chứng vú to ở nam giới) được ghi nhận chung ở < 1% bệnh nhân.
Ảnh hưởng theo nhóm thuốc
Kéo dài khoảng QT, loạn nhịp thất (rung thất, nhịp nhanh thất), đột tử không rõ nguyên nhân, ngừng tim và xoắn đỉnh có thể xảy ra trên bệnh nhân sử dụng thuốc chống loạn thần. Đã có báo cáo các trường hợp thuyên tắc huyết khối tĩnh mạch, bao gồm tắc mạch phổi và huyết khối tĩnh mạch sâu trên bệnh nhân sử dụng thuốc chống loạn thần (chưa rõ tần suất).
Báo cáo các trường hợp nghi ngờ phản ứng có hại
Báo cáo các trường hợp nghi ngờ phản ứng có hại sau khi thuốc được phép lưu hành là điều quan trọng. Điều này cho phép tiếp tục theo dõi cân bằng lợi ích/nguy cơ của sản phẩm. Nhân viên y tế được yêu cầu báo cáo bất kỳ phản ứng có hại nghi ngờ có liên quan thông qua hệ thống báo cáo quốc gia.
Thông báo ngay cho bác sỹ hoặc dược sỹ những phản ứng có hại gặp phải khi sử dụng thuốc.
6. Lưu ý |
- Thận trọng khi sử dụngSử dụng thuốc trên bệnh nhân đang ở trạng thái bị kích động cấp tính hoặc loạn thần nặng Không nên sử dụng INVEGA SUSTENNA để điều trị trạng thái bị kích động cấp tính hoặc loạn thần nặng khi cần kiểm soát triệu chứng tức thì. Khoảng QT Cần thận trọng khi kê đơn paliperidone cho bệnh nhân đã biết có bệnh lý tim mạch hoặc tiền sử gia đình có hội chứng QT kéo dài, và đang sử dụng đồng thời các thuốc khác được biết gây kéo dài khoảng QT. Hội chứng ác tính do thuốc an thần kinh Hội chứng ác tính do thuốc an thần kinh (NMS-Neuroleptic Malignant Syndrome), đặc trưng bởi tình trạng tăng thân nhiệt, cứng cơ, thần kinh thực vật không ổn định, rối loạn ý thức và tăng nồng độ creatine phosphokinase trong huyết thanh được báo cáo xảy ra khi sử dụng paliperidone. Các dấu hiệu lâm sàng khác có thể bao gồm myoglobin niệu (tiêu cơ vân cấp) và suy thận cấp. Phải ngừng sử dụng paliperidone nếu bệnh nhân xuất hiện các triệu chứng và dấu hiệu biểu thị NMS. Rối loạn vận động muộn/triệu chứng ngoại tháp Các thuốc có đặc tính kháng thụ thể dopamine liên quan đến sự khởi phát rối loạn vận động muộn đặc trưng bởi các vận động không tự chủ, có tính chất lặp lại đều đặn, chủ yếu là ở lưỡi và/hoặc mặt. Nếu xuất hiện dấu hiệu và triệu chứng rối loạn vận động muộn, phải cân nhắc ngừng dùng tất cả các thuốc chống loạn thần, bao gồm paliperidone. Đảm bảo thận trọng ở bệnh nhân dùng đồng thời các thuốc kích thần (như methylphenidate) và paliperidone, vì các triệu chứng ngoại tháp có thể xuất hiện khi điều chỉnh một hoặc cả hai thuốc. Khuyến cáo ngừng từ từ các thuốc kích thần. Giảm bạch cầu, giảm bạch cầu trung tính, và mất bạch cầu hạt Đã có báo cáo về các biến cố giảm bạch cầu, giảm bạch cầu trung tính và mất bạch cầu hạt khi dùng INVEGA SUSTENNA. Đã có báo cáo mất bạch cầu hạt với tần suất rất hiếm gặp (<1/10 000 bệnh nhân) trong giai đoạn giám sát sau khi lưu hành thuốc. Bệnh nhân có tiền sử số lượng bạch cầu thấp có ý nghĩa lâm sàng hoặc giảm bạch cầu/bạch cầu trung tính do thuốc cần được giám sát điều trị trong vài tháng đầu tiên dùng INVEGA SUSTENNA và cần ngừng thuốc ngay nếu có dấu hiệu đầu tiên của tình trạng giảm bạch cầu có ý nghĩa lâm sàng mà không có yếu tố gây bệnh nào khác. Bệnh nhân có bạch cầu trung tính giảm có ý nghĩa lâm sàng cần được theo dõi cẩn thận về tình trạng sốt hoặc các triệu chứng hoặc dấu hiệu nhiễm trùng và phải điều trị ngay nếu các triệu chứng hoặc dấu hiệu đó xuất hiện. Phải ngừng dùng INVEGA SUSTENNA khi bệnh nhân giảm bạch cầu trung tính nặng (số lượng bạch cầu trung tính tuyệt đối < 1 x 109/L) và theo dõi cho đến khi lượng bạch cầu trở lại bình thường. Phản ứng quá mẫn Hiếm có báo cáo về các phản ứng quá mẫn ở bệnh nhân đã từng dung nạp risperidone hoặc paliperidone đường uống theo kinh nghiệm sau khi lưu hành thuốc. Nếu phản ứng quá mẫn xảy ra, ngừng sử dụng INVEGA SUSTENNA; bắt đầu các biện pháp hỗ trợ phù hợp trên lâm sàng và theo dõi bệnh nhân cho đến khi các dấu hiệu và triệu chứng được giải quyết. Tăng đường huyết và đái tháo đường Đã có các báo cáo tăng đường huyết, đái tháo đường và tình trạng nặng lên của bệnh đái tháo đường sẵn có bao gồm hôn mê do đái tháo đường và nhiễm toan ceton trong khi điều trị paliperidone. Đề nghị theo dõi lâm sàng phù hợp theo hướng dẫn sử dụng các thuốc chống loạn thần. Cần theo dõi các triệu chứng của tăng đường huyết (như khát nhiều, tiểu nhiều, ăn nhiều và mệt mỏi) khi bệnh nhân điều trị INVEGA SUSTENNA và nên theo dõi thường xuyên bệnh nhân mắc đái tháo đường về tình trạng xấu đi của kiểm soát đường huyết. Tăng cân Đã có báo cáo tăng cân đáng kể khi sử dụng INVEGA SUSTENNA. Nên theo dõi cân nặng thường xuyên. Sử dụng thuốc trên bệnh nhân có khối u phụ thuộc prolactin Các nghiên cứu trên mô nuôi cấy cho thấy prolactin có thể kích thích sự tăng trưởng tế bào của các khối ung thư vú trên người. Mặc dù cho đến nay, các nghiên cứu lâm sàng và dịch tễ chưa chứng minh được mối liên quan rõ ràng với sử dụng thuốc chống loạn thần, khuyến cáo thận trọng khi sử dụng trên bệnh nhân có tiền sử bệnh lý liên quan. Nên dùng paliperidone thận trọng ở bệnh nhân đã có khối u phụ thuộc prolactin. Hạ huyết áp tư thế Paliperidone có thể gây hạ huyết áp tư thế trên một số bệnh nhân do hoạt tính chẹn thụ thể alpha. Dựa trên dữ liệu gộp từ 3 thử nghiệm có đối chứng giả dược, theo dõi trong 6 tuần, sử dụng liều cố định paliperidone đường uống viên nén giải phóng kéo dài (3, 6, 9 và 12 mg), đã ghi nhận hạ huyết áp tư thế trên 2,5% bệnh nhân điều trị paliperidone đường uống so với 0,8% bệnh nhân trong nhóm dùng giả dược. Thận trọng khi dùng INVEGA SUSTENNA trên bệnh nhân có bệnh lý tim mạch (như suy tim, nhồi máu cơ tim hoặc thiếu máu cục bộ cơ tim, rối loạn dẫn truyền), bệnh lý mạch não, hoặc những tình trạng làm tăng nguy cơ bệnh nhân hạ huyết áp (như mất nước và giảm thể tích tuần hoàn). Co giật Thận trọng khi sử dụng INVEGA SUSTENNA trên bệnh nhân có tiền sử co giật hoặc các tình trạng bệnh lý có thể làm giảm ngưỡng co giật. Suy thận Nồng độ paliperidone trong huyết tương tăng trên bệnh nhân suy thận, do đó cần lưu ý chỉnh liều cho bệnh nhân suy thận nhẹ. Không khuyến cáo sử dụng INVEGA SUSTENNA cho bệnh nhân suy thận trung bình hoặc nặng (độ thanh thải creatinine < 50 mL/phút). Suy gan Hiện chưa có dữ liệu trên bệnh nhân suy gan nặng (Child-Pugh nhóm C). Thận trọng khi dùng paliperidone cho những bệnh nhân này. Bệnh nhân cao tuổi có sa sút trí tuệ INVEGA SUSTENNA chưa được nghiên cứu trên bệnh nhân cao tuổi có sa sút trí tuệ. Thận trọng khi dùng INVEGA SUSTENNA trên bệnh nhân cao tuổi sa sút trí tuệ có các yếu tố nguy cơ đột quỵ. Kinh nghiệm từ risperidone dưới đây được xem có giá trị đối với paliperidone. Tỷ lệ tử vong chung Trong một phân tích gộp của 17 thử nghiệm lâm sàng có đối chứng, bệnh nhân cao tuổi sa sút trí tuệ được điều trị bằng các thuốc chống loạn thần không điển hình khác, bao gồm risperidone, aripiprazole, olanzapine, và quetiapine đã có tăng nguy cơ tỷ lệ tử vong so với giả dược. Tỷ lệ tử vong là 4% ở nhóm dùng risperidone so với 3,1% ở nhóm dùng giả dược. Các phản ứng có hại trên mạch máu não Trong thử nghiệm lâm sàng ngẫu nhiên có đối chứng giả dược trên bệnh nhân sa sút trí tuệ dùng một số thuốc chống loạn thần không điển hình bao gồm risperidone, aripiprazole, và olanzapine, đã thấy nguy cơ xảy ra các phản ứng có hại trên mạch máu não tăng khoảng 3 lần. Vẫn chưa biết cơ chế của tăng nguy cơ này. Bệnh Parkinson và bệnh sa sút trí tuệ thể Lewy Bác sĩ điều trị cần cân nhắc lợi ích so với nguy cơ khi kê đơn INVEGA SUSTENNA cho bệnh nhân mắc bệnh Parkinson hoặc sa sút trí tuệ thể Lewy (Dementia with Lewy Bodies – DLB) do cả hai nhóm bệnh nhân này đều có thể tăng nguy cơ mắc hội chứng ác tính do thuốc an thần kinh cũng như tăng nguy cơ nhạy cảm với các thuốc chống loạn thần. Biểu hiện của hiện tượng tăng nhạy cảm bao gồm lú lẫn, giảm ý thức, mất thăng bằng tư thế và thường xuyên té ngã, cùng các triệu chứng ngoại tháp. Chứng cương dương Đã có báo cáo các thuốc chống loạn thần (bao gồm cả risperidone) có tác dụng chẹn thụ thể alpha-adrenergic gây chứng cương dương. Trong giai đoạn giám sát sau khi lưu hành thuốc, chứng cương dương cũng được báo cáo khi dùng paliperidone đường uống là chất chuyển hóa có hoạt tính của risperidone. Nên thông báo cho bệnh nhân biết để được chăm sóc y tế khẩn cấp trong trường hợp tình trạng cương dương không thuyên giảm trong vòng 4 giờ. Điều hòa thân nhiệt Rối loạn khả năng cơ thể tự điều chỉnh giảm thân nhiệt là thuộc tính của các thuốc chống loạn thần. Nên có chế độ chăm sóc phù hợp khi kê đơn INVEGA SUSTENNA cho bệnh nhân sẽ xuất hiện những tình trạng có thể gây tăng thân nhiệt như tập thể lực tích cực, tiếp xúc với môi trường rất nóng, đang dùng đồng thời với các thuốc có hoạt tính kháng cholinergic hoặc đang trong tình trạng mất nước. Thuyên tắc huyết khối tĩnh mạch Đã có báo cáo về các trường hợp thuyên tắc huyết khối tĩnh mạch (Venous thromboembolism - VTE) khi dùng thuốc chống loạn thần. Bệnh nhân điều trị thuốc chống loạn thần thường có các yếu tố nguy cơ mắc VTE, nên cần nhận biết tất cả các yếu tố nguy cơ có thể xảy ra VTE trước khi và trong khi điều trị với INVEGA SUSTENNA và thực hiện các biện pháp phòng ngừa. Tác dụng chống nôn Đã quan sát thấy tác dụng chống nôn trong các nghiên cứu tiền lâm sàng của paliperidone. Nếu tác dụng này biểu hiện trên người, có thể che lấp các dấu hiệu và triệu chứng quá liều của thuốc nào đó hoặc các bệnh lý như tắc ruột, hội chứng Reye và u não. Cách dùng thuốc Cần thận trọng để tránh vô ý tiêm INVEGA SUSTENNA vào mạch máu. Hội chứng nhão mống mắt trong phẫu thuật nội nhãn Hội chứng nhão mống mắt trong phẫu thuật nội nhãn (Intraoperative Floppy Iris Syndrome- IFIS) đã được quan sát thấy trong phẫu thuật đục thủy tinh thể trên bệnh nhân sử dụng các thuốc có tác dụng đối kháng thụ thể alpha 1a-adrenergic như INVEGA SUSTENNA. IFIS có thể làm tăng nguy cơ biến chứng mắt trong và sau phẫu thuật. Trước khi phẫu thuật, nên thông báo cho bác sỹ phẫu thuật nhãn khoa biết đã hoặc đang dùng thuốc có tác dụng đối kháng alpha 1a-adrenergic. Chưa xác định được lợi ích tiềm tàng khi ngừng liệu pháp chẹn thụ thể alpha 1 trước khi phẫu thuật đục thủy tinh thể và phải đánh giá lợi ích so với nguy cơ ngừng liệu pháp chống loạn thần. Tá dược Thuốc này chứa natri ít hơn 1 mmol (23 mg) trên một đơn vị liều, tức là gần như không có natri. - Thời kỳ mang thai và cho con búPhụ nữ có thai Chưa có đủ dữ liệu về sử dụng paliperidone trong thai kỳ. Tiêm bắp paliperidone palmitate và uống paliperidone không gây quái thai trong các nghiên cứu trên động vật, nhưng các dạng độc tính trên sinh sản khác đã được ghi nhận (xem mục 5.3). Trẻ sơ sinh phơi nhiễm với paliperidone trong 3 tháng cuối thai kỳ có nguy cơ gặp phản ứng có hại bao gồm triệu chứng ngoại tháp và/hoặc các triệu chứng cai thuốc với mức độ nặng và khoảng thời gian kéo dài sau khi sinh có thể khác nhau. Đã có báo cáo về tình trạng kích động, tăng trương lực cơ, giảm trương lực cơ, run, ngủ gà, suy hô hấp hoặc rối loạn cho ăn. Do đó, cần theo dõi cẩn thận trẻ sơ sinh. Không sử dụng INVEGA SUSTENNA trong thai kỳ trừ khi thực sự cần thiết. Phụ nữ cho con bú Paliperidone được bài tiết vào sữa mẹ với mức độ ảnh hưởng lên trẻ bú mẹ tương tự như khi dùng liều điều trị cho mẹ. Do đó, không sử dụng INVEGA SUSTENNA khi phụ nữ đang cho con bú. Khả năng sinh sản Không quan sát thấy các tác dụng liên quan trong các nghiên cứu phi lâm sàng. - Khả năng lái xe, vận hành máy mócPaliperidone có thể ảnh hưởng mức độ nhẹ hoặc trung bình lên khả năng lái xe và vận hành máy móc do khả năng tác động trên hệ thần kinh và thị giác như an thần, ngủ gà, ngất, nhìn mờ. Do đó, cần khuyên bệnh nhân không nên lái xe hoặc vận hành máy móc cho đến khi đã biết rõ mức độ nhạy cảm của mỗi cá thể với INVEGA SUSTENNA. - Tương tác thuốcThận trọng khi kê đơn INVEGA SUSTENNA cùng với các thuốc được biết gây kéo dài khoảng QT, như thuốc điều trị rối loạn nhịp tim nhóm IA (như quinidine, disopyramide) và rối loạn nhịp tim nhóm III (như amiodarone, sotalol), một số thuốc kháng histamine, một số thuốc chống loạn thần khác và một số thuốc điều trị sốt rét (như mefloquine). Danh sách này chỉ có tính chất gợi ý và không bao gồm tất cả các loại thuốc. Ảnh hưởng của INVEGA SUSTENNA lên các thuốc khác Paliperidone được dự kiến không gây ra các tương tác dược động học quan trọng trên lâm sàng với các thuốc chuyển hóa qua isozyme cytochrome P-450. Với tác dụng chủ yếu lên thần kinh trung ương (CNS) của paliperidone, thận trọng khi kết hợp INVEGA SUSTENNA với các thuốc tác động trên thần kinh trung ương khác, như thuốc chống lo âu, đa số thuốc chống loạn thần, thuốc ngủ, các dẫn xuất opioid, … hoặc rượu. Paliperidone có thể có tác dụng đối kháng với levodopa và các chất chủ vận dopamine khác. Nếu cần phải kết hợp thuốc, đặc biệt trên bệnh nhân Parkinson giai đoạn cuối, nên kê đơn liều thấp nhất có hiệu quả của mỗi thuốc. Do khả năng gây hạ huyết áp tư thế của thuốc, có thể quan sát thấy tác dụng hiệp đồng khi dùng INVEGA SUSTENNA với thuốc khác có cùng tác dụng này, như các thuốc chống loạn thần khác, các thuốc chống trầm cảm ba vòng. Cần thận trọng khi sử dụng paliperidone kết hợp với các thuốc khác được biết là làm giảm ngưỡng co giật (như phenothiazine hoặc butyrophenone, thuốc chống trầm cảm ba vòng hoặc thuốc ức chế tái hấp thu chọn lọc serotonine - SSRI, tramadol, mefloquine, ...). Uống paliperidone viên nén giải phóng kéo dài ở trạng thái ổn định (12 mg một lần mỗi ngày) cùng với natri divalproex viên nén giải phóng kéo dài (500 mg đến 2.000 mg một lần mỗi ngày) không làm ảnh hưởng đến dược động học ở trạng thái ổn định của valproate. Chưa tiến hành nghiên cứu tương tác thuốc giữa INVEGA SUSTENNA và lithium, tuy nhiên khó có khả năng xảy ra tương tác dược động học. Ảnh hưởng của các thuốc khác lên INVEGA SUSTENNA Các nghiên cứu in vitro cho thấy CYP2D6 và CYP3A4 có thể tham gia rất ít vào quá trình chuyển hóa của paliperidone, nhưng không có dấu hiệu in vitro hay in vivo cho thấy các isozyme này đóng vai trò quan trọng trong sự chuyển hóa của paliperidone. Uống đồng thời paliperidone với paroxetine, một chất ức chế CYP2D6 mạnh, không cho thấy ảnh hưởng có ý nghĩa lâm sàng lên dược động học của paliperidone. Uống paliperidone viên nén giải phóng kéo dài một lần mỗi ngày với carbamazepine 200 mg, hai lần mỗi ngày làm giảm khoảng 37% giá trị trung bình của Cmax và AUC ở trạng thái ổn định của paliperidone. Mức giảm đáng kể này là do, carbamazepine dường như gây cảm ứng P-gp ở thận, làm tăng 35% độ thanh thải qua thận của paliperidone. Lượng hoạt chất chưa chuyển hóa thải trừ nguyên vẹn qua nước tiểu giảm nhẹ, gợi ý việc sử dụng đồng thời với carbamazepine ít gây ảnh hưởng tới chuyển hóa qua CYP hoặc sinh khả dụng của paliperidone. Khi dùng carbamazepine liều cao hơn, có thể xảy ra giảm nhiều hơn nồng độ paliperidone trong huyết tương. Khi bắt đầu điều trị với carbamazepine, cần đánh giá lại liều INVEGA SUSTENNA và tăng liều nếu cần. Ngược lại, khi dừng carbamazepine, cũng phải đánh giá lại liều INVEGA SUSTENNA và giảm liều nếu cần. Uống liều đơn paliperidone viên nén giải phóng kéo dài 12 mg với natri divalproex viên nén giải phóng kéo dài (2 viên 500 mg, một lần mỗi ngày) làm tăng khoảng 50% Cmax và AUC của paliperidone, dường như do tăng hấp thu qua đường uống. Do không quan sát thấy tác dụng trên thanh thải toàn thân, dường như không có tương tác có ý nghĩa lâm sàng giữa natri divalproex viên nén giải phóng kéo dài và INVEGA SUSTENNA tiêm bắp. Tương tác này chưa được nghiên cứu với INVEGA SUSTENNA. Sử dụng đồng thời INVEGA SUSTENNA với risperidone hoặc với paliperidone đường uống Do paliperidone là chất chuyển hóa chính có hoạt tính của risperidone, cần thận trọng khi sử dụng đồng thời INVEGA SUSTENNA với risperidone hoặc paliperidone đường uống trong thời gian kéo dài. Dữ liệu an toàn liên quan đến sử dụng đồng thời INVEGA SUSTENNA với các thuốc chống loạn thần khác còn hạn chế. Sử dụng đồng thời INVEGA SUSTENNA với các thuốc kích thần Sử dụng kết hợp các thuốc kích thần (như methylphenidate) với paliperidone có thể dẫn đến các triệu chứng ngoại tháp khi thay đổi một hoặc cả hai thuốc. |
7. Dược lý
- Dược lực học (Tác động của thuốc lên cơ thể)
Nhóm dược lý điều trị: Thuốc an thần, các thuốc chống loạn thần khác. Mã ATC: N05AX13
INVEGA SUSTENNA chứa hỗn hợp racemic của (+)- và (-)-paliperidone.
Cơ chế tác dụng
Paliperidone là chất đối kháng chọn lọc tác dụng của monoamine, thuốc có đặc tính dược lý khác với các thuốc an thần kinh cổ điển. Paliperidone gắn mạnh vào thụ thể serotonin 5-HT2-và thụ thể dopamine D2. Paliperidone cũng chẹn thụ thể alpha 1-adrenergic và chẹn mức độ yếu hơn thụ thể histamine H1 và alpha 2-adrenergic. Tác dụng dược lý của hai đồng phân (+)- và (-)-paliperidone tương tự nhau về mặt định tính và định lượng.
Paliperidone không gắn vào thụ thể cholinergic. Mặc dù paliperidone là chất đối kháng thụ thể D2 mạnh, được cho là làm giảm các triệu chứng dương tính của tâm thần phân liệt, thuốc ít gây tình trạng giữ nguyên tư thế, và ít làm giảm chức năng vận động hơn so với các thuốc an thần kinh cổ điển. Tác động kháng serotonin trung ương nổi trội của paliperidone có thể giảm khuynh hướng gây ra tác dụng không mong muốn ngoại tháp.
Bệnh nhân nhi
Cơ quan quản lý Dược phẩm Châu Âu đã miễn nghĩa vụ nộp kết quả nghiên cứu với
INVEGA SUSTENNA trong tất cả các phân nhóm bệnh nhân nhi bị bệnh tâm thần phân liệt.
- Dược động học (Tác động của cơ thể với thuốc)
Hấp thu và phân bố
Paliperidone palmitate là tiền thuốc dạng ester palmitate của paliperidone. Do tính tan trong nước cực thấp, paliperidone palmitate tan chậm sau khi tiêm bắp trước khi bị thủy phân thành paliperidone và hấp thu vào tuần hoàn chung. Sau khi tiêm bắp một liều duy nhất, nồng độ paliperidone trong huyết tương tăng lên dần dần để đạt nồng độ tối đa trong huyết tương với trung vị của Tmax là 13 ngày. Giải phóng hoạt chất bắt đầu ngay vào ngày 1 và kéo dài ít nhất 4 tháng.
Sau khi tiêm bắp một liều duy nhất (25-150 mg) vào cơ delta, trung bình, Cmax được ghi nhận cao hơn 28% so với tiêm vào cơ mông. Hai liều tiêm vào cơ delta ban đầu là 150 mg vào ngày 1 và 100 mg vào ngày thứ 8 giúp đạt được nồng độ điều trị nhanh chóng. Đặc tính giải phóng thuốc và phác đồ liều của INVEGA SUSTENNA giúp duy trì nồng độ điều trị. Tổng nồng độ paliperidone sau khi dùng INVEGA SUSTENNA tỷ lệ với liều trong khoảng liều 25-150 mg, và Cmax tỷ lệ với liều dùng ít hơn với các mức liều trên 50 mg. Tỷ số nồng độ đỉnh: đáy trung bình ở trạng thái ổn định của INVEGA SUSTENNA 100 mg là 1,8 sau khi tiêm vào cơ mông
và 2,2 sau khi tiêm vào cơ delta. Giá trị trung vị của thời gian bán thải biểu kiến của paliperidone sau khi dùng INVEGA SUSTENNA trong khoảng liều 25-150 mg dao động từ 25-49 ngày.
Sinh khả dụng tuyệt đối của paliperidone palmitate sau khi sử dụng INVEGA SUSTENNA là 100%.
Sau khi tiêm paliperidone palmitate, các đồng phân đối quang (+) và (-) paliperidone chuyển đổi lẫn nhau, đạt tỷ số AUC (+) và (-) khoảng 1,6 -1,8.
Liên kết protein huyết tương của paliperidone racemic là 74%.
Chuyển dạng sinh học và thải trừ
Một tuần sau khi uống một liều đơn 1 mg 14C-paliperidone giải phóng tức thì, 59% liều thải trừ nguyên vẹn qua nước tiểu, cho thấy paliperidone không được chuyển hóa rộng rãi ở gan. Khoảng 80% hoạt chất đánh dấu phóng xạ được tìm thấy trong nước tiểu và 11% trong phân. Đã xác định bốn con đường chuyển hóa thuốc trên in vivo, trong đó không có con đường nào chiếm trên 6,5% liều: dealkyl hóa, hydroxyl hóa, dehydrogen hóa, và phản ứng phân ly benzisoxazole. Mặc dù các nghiên cứu in vitro gợi ý về vai trò của CYP2D6 và CYP3A4 trong chuyển hóa paliperidone, không có bằng chứng in vivo nào cho thấy isozyme này đóng vai trò quan trọng trong chuyển hóa paliperidone. Các phân tích dược động học quần thể cho thấy không có sự khác biệt rõ ràng giữa độ thanh thải biểu kiến của paliperidone sau khi sử dụng paliperidone đường uống giữa người chuyển hóa mạnh và chuyển hóa yếu qua cơ chất của CYP2D6. Các nghiên cứu in vitro trên microsome gan người cho thấy paliperidone không ức chế đáng kể chuyển hóa của các thuốc mà bị chuyển hóa qua các isozyme của cytochrome P450, bao gồm CYP1A2, CYP2A6, CYP2C8/9/10, CYP2D6, CYP2E1, CYP3A4, và
CYP3A5.
Các nghiên cứu in vitro cho thấy paliperidone là cơ chất của protein P-gp và ức chế yếu P-gp ở nồng độ cao. Vẫn chưa có các dữ liệu in vivo và chưa biết mối liên quan trên lâm sàng.
Paliperidone palmitate thuốc tiêm tác dụng kéo dài so với paliperidone giải phóng kéo dài đường uống
INVEGA SUSTENNA được thiết kế để giải phóng paliperidone trong thời gian một tháng, trong khi dùng paliperidone giải phóng kéo dài đường uống mỗi ngày. Phác đồ liều khởi đầu cho INVEGA SUSTENNA (150 mg/100 mg vào cơ delta vào ngày 1/ngày 8) được thiết kế để nhanh chóng đạt được nồng độ paliperidone ở trạng thái ổn định khi bắt đầu điều trị mà không sử dụng thêm thuốc đường uống.
Nói chung, quan sát thấy nồng độ thuốc trong huyết tương ban đầu với INVEGA SUSTENNA nằm trong khoảng nồng độ quan sát được khi uống 6-12 mg paliperidone giải phóng kéo dài. Sử dụng phác đồ liều khởi đầu INVEGA SUSTENNA cho phép bệnh nhân duy trì trong khoảng liều 6-12 mg paliperidone giải phóng kéo dài đường uống, ngay cả khi ở nồng độ đáy vào ngày trước khi tiêm liều tiếp theo (ngày 8 và ngày 36). Do sự khác nhau về trung vị các thông số dược động học giữa hai sản phẩm, cần thận trọng khi so sánh trực tiếp đặc tính dược động học của chúng.
Suy gan
Paliperidone không chuyển hóa rộng rãi ở gan. Mặc dù INVEGA SUSTENNA không được nghiên cứu trên bệnh nhân suy gan, không cần điều chỉnh liều ở bệnh nhân suy gan nhẹ hoặc trung bình. Trong một nghiên cứu với paliperidone đường uống trên bệnh nhân suy gan trung bình (Child-Pugh nhóm B), nồng độ paliperidone tự do trong huyết tương tương tự với nồng độ của người khỏe mạnh. Paliperidone chưa được nghiên cứu ở bệnh nhân suy gan nặng.
Suy thận
Sự phân bố của một liều uống paliperidone viên nén giải phóng kéo dài 3 mg được nghiên cứu ở các đối tượng với mức độ chức năng thận khác nhau. Thải trừ paliperidone giảm khi độ thanh thải creatinine dự kiến giảm. Độ thanh thải toàn phần của paliperidone giảm trung bình 32% ở người suy thận nhẹ (CrCl = 50 đến < 80 mL/phút), 64% ở người suy thận trung bình (CrCl = 30 đến < 50 mL/phút), và 71% ở người suy thận nặng (CrCl = 10 đến < 30 mL/phút), với sự gia tăng nồng độ trung bình (AUCinf) lần lượt là 1,5; 2,6 và 4,8 lần, so với người khỏe mạnh. Dựa vào một số ít các quan sát với INVEGA SUSTENNA ở bệnh nhân bị suy thận nhẹ và mô phỏng dược động học, khuyến cáo nên giảm liều.
Người cao tuổi
Phân tích dược động học quần thể không thấy bằng chứng về sự khác biệt dược động học liên quan đến tuổi.
Chỉ số khối cơ thể (BMI)/trọng lượng cơ thể
Các nghiên cứu dược động học với paliperidone palmitate đã cho thấy nồng độ paliperidone trong huyết tương thấp hơn không đáng kể (10-20%) ở bệnh nhân thừa cân hoặc béo phì so với bệnh nhân có cân nặng bình thường.
Chủng tộc
Phân tích dược động học quần thể của dữ liệu từ các nghiên cứu với paliperidone đường uống không thấy bằng chứng về sự khác biệt trong dược động học của paliperidone liên quan đến chủng tộc sau khi sử dụng INVEGA SUSTENNA.
Giới tính
Không có sự khác biệt đáng kể có ý nghĩa lâm sàng giữa nam và nữ.
Tình trạng hút thuốc
Dựa trên các nghiên cứu in vitro sử dụng men gan người, paliperidone không phải là cơ chất của CYP1A2; do đó, hút thuốc không ảnh hưởng đến dược động học của paliperidone. Ảnh hưởng của hút thuốc lên dược động học của paliperidone chưa được nghiên cứu với INVEGA SUSTENNA. Một phân tích dược động học quần thể dựa trên dữ liệu với paliperidone viên nén giải phóng kéo dài đường uống cho thấy nồng độ paliperidone ở người hút thuốc thấp hơn không đáng kể so với người không hút thuốc. Sự khác biệt dường như không có ý nghĩa lâm sàng.
8. Thông tin thêm
- Đặc điểm
Hỗn dịch tiêm giải phóng kéo dài. Hỗn dịch có màu trắng tới trắng ngà. Hỗn dịch có pH trung tính (khoảng 7,0).
- Bảo quản
Không bảo quản ở nhiệt độ trên 30°C.
- Quy cách đóng gói
Hộp chứa 1 bơm tiêm đóng sẵn thuốc và 2 kim tiêm.
- Hạn sử dụng
24 tháng kể từ ngày sản xuất
- Nhà sản xuất
JANSSEN PHARMACEUTICA N.V.
Mã: 109016
- Bước 1: Điền vào form đang ký và bấm nút Đặt trước ở bên dưới.
- Bước 2: Trong vòng 48 giờ sau khi gửi form, dược sĩ sẽ gọi điện báo giá và thời gian nhận hàng cho Quý khách (trừ T7, CN và ngày lễ)
- Bước 3: Để mua hàng, vui lòng Đặt cọc trước 100% giá trị đơn hàng.
- Bước 4: Sau khi nhận cọc, An Khang tiến hành nhập và giao hàng đúng theo cam kết